О.Г. Шадрін, Г.А. Гайдучик
ДУ «Інститут педіатрії, акушерства та гінекології НАМН України», м. Київ, Україна
SOVREMENNAYA PEDIATRIYA.2016.1(73):111-115
Мета:
Дослідження жирно-кислотного спектра ліпідної фракції крові у дітей раннього віку з харчовою алергією (ХА) та ефективності дієтичної корекції його порушень.
Пацієнти і методи. Обстежено 45 дітей віком від 6-ти місяців до 3-х років. Усім дітям проводилося дослідження жирно-кислотного спектра ліпідної фракції крові. Діти з ХА (25 осіб) у складі комплексної терапії отримували Смарт Омега® бебі протягом місяця.
Результати. За результатами аналізу жирно-кислотного спектра ліпідної фракції цільної крові у дітей раннього віку з ХА встановлений дисбаланс жирних кислот за рахунок збільшення частки омега-6 ПНЖК, що свідчить про прозапальну спрямованість обміну ліпідів. Включення до складу комплексної терапії ХА Смарт Омега® бебі призвело до позитивних змін співвідношення омега-3/омега-6 ПНЖК. У пацієнтів основної групи спостереження відбулося зменшення розладів з боку шлунково-кишкового тракту, покращення стану шкіри.
Висновки. Враховуючи виявлені порушення співвідношення омега-3/омега-6 ПНЖК як у дітей з ХА, так і у практично здорових є обгрунтованим прийом омега 3 ПНЖК.
Ключові слова: харчова алергія, поліненасичені жирні кислоти, діти раннього віку.
Вступ
Поширеність алергічних захворювань у всьому світі набуває катастрофічних масштабів, причому як у розвинених, так і в країнах, що розвиваються. Кожні 10 років кількість людей, що мають алергічні реакції, подвоюється. Вкрай серйозною є проблема алергії у дитячому віці — за останні 20 років її поширеність у дітей раннього віку зросла до 6–10%.
Однією з причин зростання кількості алергічних захворювань є зміна способу життя та харчування населення індустріально розвинутих країн та, особливо, великих міст. Харчування сучасної людини характеризується дисбалансом між споживанням продуктів, які містять «чисті» калорії наповнювачів, солоду, пальмової олії та інших жирів, та дефіцитом у їжі вітамінів, есенціальних мінеральних речовин, природних жирів, антиоксидантів, незамінних амінокислот.
У продуктах харчування з’явились компоненти, зокрема трансжирні кислоти, замінники цукру, поліпшувачі запаху, смаку, забарвлення, консистенції, яких людина раніше не знала, і ферментні системи організму не адаптовані до цих речовин. Змінився не лише склад, але і якість харчових продуктів. Збільшення кількості таких харчових продуктів, як солодощі, та продуктів з високим вмістом насичених жирів призводить до росту ендокринних захворювань — діабету та ожиріння, зниження захисних властивостей імунної системи. З іншого боку, значне зменшення в раціоні продуктів, збагачених антиоксидантами та омега-3 жирними кислотами, є причиною зміни імунологічної відповіді, активізації систем, які беруть участь у розвитку алергічних та автоімунних захворювань [8,9].
Поліненасичені жирні кислоти (ПНЖК) належать до числа незамінних факторів харчування та є предметом вивчення вітчизняних і зарубіжних дослідників. За останні десятиріччя накопичений великий обсяг наукових даних, які вказують на важливу роль цих сполук у реалізації численних фізіологічних та біохімічних процесів в організмі як в нормі, так і при патологічних станах, зокрема у формуванні імунного статусу, запальних реакціях, регуляції системи гемостазу, підтримці тонусу судин та гладких м’язів, процесів росту, когнітивних функцій [3,4,6,7,11]. Разом з тим встановлено, що при метаболізмі довголанцюгових ПНЖК в організмі утворюються ліпідні медіатори алергії — простагландини, лейкотрієни, тромбоксани та ін.., причому з різних видів ПНЖК утворюються різні класи ліпідних медіаторів, які відрізняються за своєю активністю.
Так, метаболіти омега-6 ЖК — лейкотрієни 4 серії мають прозапальні властивості, натомість метаболіти омега-3 ПНЖК — лейкотрієни 5 серії, навпаки, проявляють виразні протизапальні характеристики. У зв’язку з цим ПНЖК розглядають як потужний аліментарний фактор, здатний суттєво впливати на регуляцію метаболічних процесів в організмі. Вивченню можливих профілактичних та лікувальних ефектів омега-3 ПНЖК присвячено декілька досліджень у дорослих, які показують, що важливу роль у розвитку алергічних реакцій відіграє зменшення вмісту у сироватці крові омега-3 ПНЖК та збільшення співвідношення ПНЖК омега-6/омега-3, що підтримує хронічне алергічне запалення [5,10,12].
Ключовим представником омега-6 ПНЖК є арахідонова кислота (АК), яка входить до складу фосфоліпідів клітинних мембран тромбоцитів та ендотеліальних клітин. Вільна АК швидко метаболізується, перетворюючись на простагландини та тромбоксани. Метаболізм АК відбувається двома основними шляхами — циклооксигеназним та ліпооксигеназним. Циклооксигеназний шлях метаболізму АК призводить до утворення простагландинів та тромбоксану А2, ліпооксигеназний — до утворення лейкотрієнів. Арахідонова кислота частково потрапляє з їжею (рослинні олії), частково синтезується в організмі, що забезпечує її постійну присутність. При достатньому надходженні до організму омега-3 ПНЖК витісняють АК та вступають у конкурентне заміщення АК у фосфоліпідах клітинних мембран у циклооксигеназному та ліпооксигеназному шляхах метаболізму, тобто синтезі ейкозаноїдів з омега-6 ПНЖК та омега-3 ПНЖК. Функціональні властивості ейкозаноїдів, які синтезуються з омега-6 ПНЖК та омега-3 ПНЖК, значною мірою протилежні.
Конкуренція між АК та омега-3 ПНЖК на циклооксигеназно-ліпооксигеназному рівні проявляється модифікацією спектра простагландінів та лейкотрієнів.
В останні 150 років ми спостерігаємо безпрецедентні зміни у споживанні корисних жирів. Рафіновані олії (кукурудзяна, соєва, соняшникова) витісняють жири, які отримують з риби, дичини і диких рослин. Співвідношення ПНЖК омега-6 до омега-3 в сучасному раціоні підвищилося від 1:1 до 10:1–20:1, що призвело до негативних наслідків. Ріст практично всіх основних вікових захворювань фахівці напряму пов’язують із дисбалансом ЖК у раціоні.
Центральну роль у підтримці гомеостазу запальних реакцій відіграють омега-3 ПНЖК — ЕПК і ДГК. ЕПК є попередником тромбоксанів, простагландинів і лейкотрієнів — високоактивних імунозапальних регуляторів.
Крім того, нещодавно описані окислені метаболіти ЕПК і ДГК — резолвіни, докозатрієни і нейропротектини, які мають протизапальні і захисні властивості. Наш організм здатен синтезувати ДГК та ЕПК з рослинної коротколанцюгової альфа-линоленової кислоти, однак цей процес недосконалий та може блокуватись при надмірному вживанні омега-6 ПНЖК. До 25% ПНЖК головного мозку представлені ДГК, яка регулює процеси росту головного мозку плода в останньому триместрі вагітності [6]. ДГК становить біля 50% усіх ЖК сітківки та забезпечує нормальне функціонування фоторецепторів, що визначає гостроту зору. Недостатнє надходження ДГК під час вагітності призводить до погіршення розвитку когнітивних функцій та зору [7,11]. Омега-3 ПНЖК забезпечують імунні функції в організмі шляхом синтезу ейкозаноїдів, контролюючи інтенсивність та тривалість запальних реакцій. Метаболіти ДГК знижують активність запальних та імунних реакцій, інгібуючи ІЛ-6, ІЛ-8 і фактор некрозу пухлин β, сприяючи тим самим формуванню харчової толерантності.
Накопичення ЕПК і ДГК у тканинах є найбільш ефективним, коли вони надходять безпосередньо з їжею або коли конкуруючі кількості омега-6 аналогів є низькими.
У сучасному світі реальним джерелом омега-3 ПНЖК є морська риба (лосось, форель, макрель, оселедець, тунець), жир морських ссавців, морські водорості, курячі домашні яйця, насіння льону та лляна олія. Слід зазначити, що найбільш корисна риба у сирому та слабосолоному вигляді, оскільки під час приготування страв більшість омега-3 ПНЖК руйнуються. Лляна олія містить альфа-линоленову кислоту, яка руйнується при термічній обробці, тому олія повинна бути тільки холодного віджиму і використовуватись лише для заправки страв. Невелику кількість омега-3 ПНЖК містять волоські горіхи, насіння гарбуза, соєва, рапсова та оливкова олії, а також петрушка, кріп, кіндза, портулак.
Нещодавні дослідження продемонстрували зниження частоти алергічних захворювань у дітей в перші чотири роки життя за умов збагачення раціону харчування впродовж грудного віку риб’ячим жиром [9,13]. Вважається, що ейкозаноїди, які синтезуються з ЕПК, є менш активними, ніж синтезовані з омега-6 ПНЖК. Це означає, що вживання матір’ю під час вагітності їжі, збагаченої ЕПК, сприятиме формуванню менш алергенної імунної системи плоду [8]. Результати декількох рандомізованих контрольованих досліджень довели, що вживання матір’ю 0,2–3,7 г ДГК та EПК на добу знижує ризик розвитку харчової алергії та екземи у дитини, покращує психічний розвиток, візуально-рухову координацію та гостроту зору [8,9,11,13]. Позитивний вплив додаткового прийому омега-3 ПНЖК (0,3–0,6 г/добу) відмічений серед дітей із синдромом дефіциту уваги з гіперактивністю [12].
У США Комітетом харчових продуктів та харчування рекомендовано споживання омега-3 ПНЖК для дітей дошкільного віку 0,15 г/добу, а ВООЗ — 0,1–0,25 г/добу залежно від віку [5].
Таким чином, за допомогою сучасного харчового раціону досить складно отримати необхідну кількість омега-3 ПНЖК. Ситуація ускладнюється широким використанням у харчовому виробництві кулінарних жирів, маргаринів, рослинних олій, трансжирів, які містять багато омега-6 ЖК, що на тлі зниженого вживання омега-3 ПНЖК поглиблює дисбаланс між квотою омега-6 та омега-3 ПНЖК у бік збільшення надходження в організм омега-6 ПНЖК. Така ситуація впливає на перебіг багатьох хронічних захворювань, у тому числі й харчової алергії. Вирівняти вказаний дисбаланс дозволить додатковий прийом омега-3 ПНЖК.
Метою роботи було вивчення жирно-кислотного спектра ліпідної фракції крові у дітей раннього віку з харчовою алергією та ефективності дієтичної корекції його порушень.
Матеріал і методи дослідження
Обстежено 45 дітей віком від 6-ти місяців до 3-х років, які перебували на обстеженні та лікуванні у відділенні проблем харчування та соматичних захворювань дітей раннього віку ДУ «ІПАГ НАМН України»: 25 хворих на харчову алергію (ХА) склали основну групу та 20 — контрольну. Середній вік пацієнтів на момент проведення дослідження становив 1,3±0,2 року.
Критеріями включення були ранній вік та наявність гастроінтестинальних і шкірних проявів ХА. Діагноз встановлювали на підставі даних алергологічного анамнезу, наявності гастроінтестинальних проявів ХА (болі у животі, блювота, здуття живота, діарея, закрепи), алергічних проявів з боку інших органів і систем (шкіра, очі, ніс, легені), наявності сенсибілізації до харчових алергенів, підвищення рівня еозинофільного катіонного білка у сироватці крові та позитивного клінічного ефекту від елімінації «причинного» алергену.
Кількісне визначення вмісту жирних кислот у крові проводили методом капілярної газової хроматографії.
Екстракцію жирних кислот ліпідної фракції цільної венозної крові проводили методом Блайя—Дайера. Хроматографування метилових ефірів жирних кислот проводили на газовому хроматографі «Кристаллюкс-4000М» з полум’яно-іонізаційним детектором у визначених нами оптимальних умовах газохроматографічного розділення та кількісного визначення. Розділення досліджуваних речовин проводилось на капілярній колонці Zebron ZB-WAX з поліетиленгликолем. Обробка хроматографічної інформації проводилась за допомогою програми Netchromwin. За результатами роботи був визначений склад та відсоткове співвідношення жирних кислот у ліпідній фракції цільної венозної крові дітей основної та контрольної груп спостереження.
Хворі отримували базисну терапію відповідно до рекомендацій Керівництва NIAID (The National Institute of Allergy and Infectious Diseases — Національний інститут алергії та інфекційних захворювань) з діагностики та лікування ХА в США — «Guidelines for the Diagnosis and Management of Food Allergy in the United States: Report of the NIAID-Sponsored Expert Panel» (The Journal of Allergy and Clinical Immunology, Vol. 126, Issue 6, Suppl., Pages S1-S58, December 2010), яка включала: елімінаційну дієту, антигістамінні, ферментні препарати, антилейкотрієнові препарати і топічні глюкокортикостероїди за показаннями [1,2].
Діти з ХА у складі комплексної терапії отримували Смарт Омега® бебі (SCHONEN, Швейцарія—Великобританія) протягом місяця у дозі 5 мл (1 чайна ложка) 1 раз на день під час їди з наступним контролем ефективності корекції шляхом визначення жирно-кислотного спектра ліпідної фракції цільної крові в динаміці на 30-й день прийому дієтичної добавки. Клінічна ефективність застосування Смарт Омега® бебі оцінювалась за інтенсивністю клінічних проявів з боку шлунково-кишкового тракту та шкіри, динамікою активності алергічного запалення в динаміці.
В якості джерела омега-3 ПНЖК було обрано Смарт Омега® бебі за рахунок зручної форми випуску для дітей раннього віку. Смарт Омега® бебі випускається у вигляді масляного розчину у флаконах 100 мл і містить у своєму складі риб’ячий жир з тушок океанічних риб (омега-3 ПНЖК), 5 мл розчину містять: вітамін А — 400 мкг, вітамін D3 — 5 мкг, вітамін Е — 5 мг, екстракт плодів лимона. Енергетична цінність на 100 мл становить 3472 кДж/830 ккал. Смарт Омега® бебі рекомендована для використання у раціоні харчування дітей як додаткове джерело незамінних омега-3 ПНЖК (ЕПК/ДГК) та жиророзчинних вітамінів А, D3, Е з метою створення оптимальних дієтологічних умов функціонування когнітивної, нервової та кістково-м’язової систем у період інтенсивного росту і розвитку.
Результати дослідження та їх обговорення
Обтяжений сімейний алергологічний анамнез відмічений у 2/3 дітей з ХА: у 9 (36,0%) — по материнській лінії, у 6 (24,0%) — по лінії батька, у 5 (20,0%) — обоє батьків мали алергічні захворювання.
Клінічно харчова алергія у обстежених дітей мала прояви з боку шлунково-кишкового тракту та шкіри. Найчастіше зустрічалось поєднання гастроінтестинального та шкірного синдрому — у 44,0% дітей; ізольовані гастро-інтестинальні прояви ХА відмічено у 16,0% пацієнтів.
Ізольований шкірний синдром був наявний у 20,0% дітей.
Ураження шкіри характеризувалось хронічним рецидивним перебігом з переважанням еритематозно-сквамозних середньоважких форм (сухість, лущення, еритема, екскоріації). Середній показник індексу SCORAD — 30 балів.
Гастроінтестинальні прояви ХА характеризувались абдомінальним больовим, диспепсичним та дискінетичним синдромами.
На початку лікування больовий абдомінальний синдром відмічався у 60,0% дітей. Частота реєстрації диспепсичного та дискінетичного синдромів становила 68,0% та 60,0% відповідно.
У всіх обстежених виявлена сенсибілізація до харчових алергенів: у 2/3 — до білків коров’ячого молока, у 8 — до яєчного білка, у 11 виявлена сенсибілізація до алергену пшеничного борошна. Сенсибілізацію до двох та більше харчових алергенів мали семеро обстежених.
Рівень загального IgE сироватки понад 2–3 норми виявлено лише у дев’яти обстежених, середнє значення загального IgE склало 68,6 IU/ml при референтних значеннях (<45 IU/ml). Еозинофільний катіонний білок (ЕКБ) сироватки крові був підвищений у більшості обстежених, середній показник його склав 78,5 нг/мл (при нормі 0–24 нг/мл). Аналіз параклінічних даних дітей з ХА показав зміни з боку червоної крові у вигляді гіпохромної анемії та незначної еозинофілії у 56,0% обстежених.
Під час дослідженні жирно-кислотного спектра крові дітей з ХА привертає увагу тенденція до збільшення вмісту насичених (НЖК) та зменшення ненасичених жирних кислот (НеНЖК) (табл.). Співвідношення НеНЖК/НЖК у дітей з ХА — 0,78, у пацієнтів контрольної групи спостереження — 1,07. Співвідношення НЖК/ПНЖК у дітей з ХА — 2,17, в контрольній групі — 1,62. Фізіологічна дія цих кислот в організмі значною мірою є протилежною. Ненасичені жирні кислоти беруть участь у побудові клітинних та субклі тинних мембран, зменшують їх плинність та підвищують в’язкість, що супроводжується помірною схильністю до перекисного окислення та підвищенням згортання крові. Ненасичені жирні кислоти знижують в’язкість і підвищують плинність мембран, знижують згортання та вміст холестерину в крові.
Ненасичених жирні кислоти знижують в’язкість і підвищують плинність мембран, знижують згортання та вміст холестерину в крові. Виявлені зміни насиченості ЖК, що зазвичай відбуваються при активації процесів ліпідної пероксидації, супроводжуються зменшенням ПНЖК. Насичені і ненасичені ЖК плазми необхідні мембранам клітин для нормального функціонування та використовуються не тільки для підтримки їх структури, але і як попередники синтезу біологічно активних сполук. Отримані дані свідчать про можливість використання довголанцюгових жирних кислот для корекції структури і в’язкості мембран клітин.
Паралельно до зменшення концентрації НеНЖК знижується концентрація ПНЖК, причому в структурі ПНЖК збільшується частка омега-6 фракції та її основного представника — АК. Наявна тенденція до збільшення рівня попередника омега-6 ПНЖК — лінолевої кислоти. Під час аналізу рівня АК привертає увагу тенденція до підвищення її концентрації у пацієнтів основної групи порівняно зі здоровими дітьми. Виявлені зміни у концентрації омега-6 ПНЖК — лінолевої (ЛК) та її похідної — АК, за даними літератури, визначають прозапальну спрямованість ліпідного спектра сироватки крові. Зважаючи, що на рівень зазначених кислот впливає як наявність у раціоні рослинних олій і тваринних жирів, так і синтез АК із ЛК, який значною мірою залежить від вмісту омега-3 ПНЖК в організмі, ми визначали співвідношення АК та ЛК [3].
У дітей контрольної групи коефіцієнт К склав 0,24, а у дітей основної групи — 0,26.
При аналізі рівня омега-3 ПНЖК у дослідних групах виявлено, що їх концентрація у дітей раннього віку з ХА практично не відрізняється від спектра у здорових дітей.
Аналіз отриманих результатів хроматографічного дослідження виявив низький рівень вмісту омега-3 ПНЖК та високі концентрації омега-6 ПНЖК у пацієнтів обох груп спостереження. Співвідношення в контрольній групі становило 1:14 (що не є оптимальним, згідно з рекомендаціями ВООЗ), а в групі дітей з ХА — 1:19 (рис.).
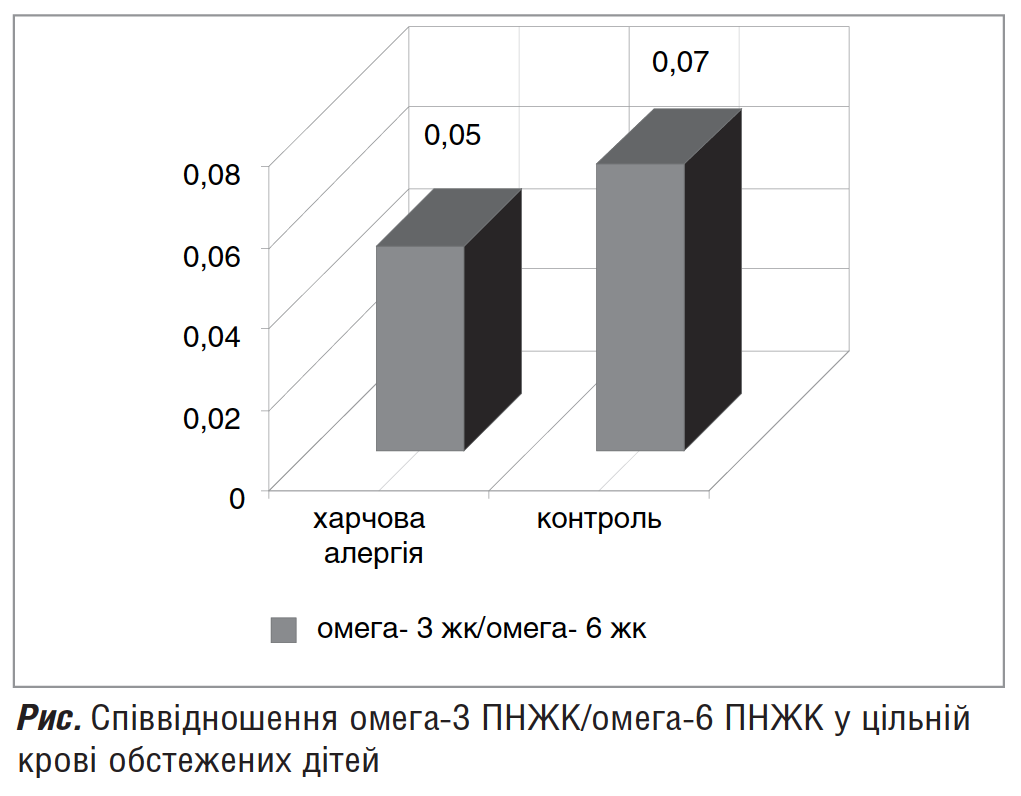
Таким чином, виявлений дисбаланс ЖК у сироватці крові дітей раннього віку з ХА за рахунок збільшення частки омега-6 ПНЖК свідчить про прозапальну спрямованість обміну ліпідів.
Враховуючи описану нами вище роль співвідношення омега-3 ПНЖК/омега-6 ПНЖК у патогенезі ХА, ми провели корекцію жирно-кислотного спектра у дітей з ХА шляхом призначення їм Смарт Омега® бебі у складі комплексної терапії.
Після місячного курсу комплексної терапії з включенням Смарт Омега® бебі у пацієнтів основної групи спостереження відбулося зменшення розладів з боку шлунково-кишкового тракту — зменшення частоти дискінетичного (з 68,0% до 16,0%) та диспепсичного синдромів (з 60,0% до 20,0%) та поліпшення стану шкіри — достовірне зниження середнього балу за шкалою SCORAD з 32 балів на початку лікування до 10 балів відповідно. Відмічено достовірне зниження концентрації ECP у сироватці крові як показника активності алергічного запалення, практично до нормальних значень (28,6±1,5 проти 78,5±2,8 нг/мл).
Корекція жирно-кислотного спектра ліпідної фракції крові дітей раннього віку з ХА за допомогою Смарт Омега® бебі призвела до позитивних змін ліпідного спектра крові: достовірно збільшилась концентрація омега-3 ПНЖК (з 1,45% до 2,9%) та знизився рівень омега-6 ПНЖК (з 28,45% до 20,12%), що призвело до достовірного зниження співвідношення омега-3/омега-6 ПНЖК — 1:7 порівняно з 1:19 на початку корекції.
З метою досягнення більш виразного впливу на співвідношення омега-3/омега-6 ПНЖК, ймовірно, необхідний триваліший курс прийому дієтичної добавки, яка містить у своєму складі омега-3 ПНЖК.
Індивідуальна переносимість Смарт Омега була хорошою у всіх 25 дітей основної групи. У процесі виконання дослідження не спостерігалося негативних реакцій на прийом дієтичної добавки, у тому числі не виявлено алергічних реакцій або посилення клінічної симптоматики захворювання у дітей з ХА.
Висновки
1. За результатами аналізу жирно-кислотного спектра ліпідної фракції цільної крові дітей раннього віку з ХА встановлений дисбаланс жирних кислот за рахунок збільшення частки омега-6 ПНЖК, що свідчить про прозапальну спрямованість обміну ліпідів.
2. Включення до складу комплексної терапії дітей раннього віку з ХА Смарт Омега® бебі з метою корекції жирно-кислотного спектра крові призвело до позитивних змін співвідношення омега-3/омега-6 ПНЖК.
3. Враховуючи виявлені порушення співвідношення омега-3/омега-6 ПНЖК у практично здорових дітей, рекомендовано призначення з профілактичною метою дітям раннього віку омега-3 ПНЖК.
ЛІТЕРАТУРА
1.Клыкова Т. В. Пищевая аллергия у детей раннего возраста: подходы к диагностике и лечению / Т. В. Клыкова, Е. В. Агафонова, И. Д. Решетникова // Практич. медицина. — 2011. — № 51. — С. 125—131.
2.Осообливості діагностики та підходи до лікувально-профілактичного харчування дітей раннього віку з алергією до білка коров’ячого молока: методичні рекомендації / Шадрін О.Г., Няньковський С.Л., Добрянський Д.О. [та ін.]. — Київ, 2014. — 28 с.
3.Сороколєтова А. Б. Клініко-патогенетичне обгрунтування застосування омега-3 поліненасичених жирних кислот при затяжному перебігу діареї у дітей раннього віку: дис. … канд. мед. наук : 14.01.10 / А. Б. Сороколєтова. — Київ, 2008. — 152 с.
4.Шадрин О. Г. Нарушения жирнокислотного спектра крови и пути его коррекции у детей с врожденными гепатитами / О. Г. Шадрин, Н. Ф. Чернега, Р. В. Марушко // Современная педиатрия. — 2014. — № 8 (64). — С. 98—103.
5.Обзор образа питания и качества потребляемой пищи / Nelson M. [и др.]. — Т. 2 : Объем потребляемой пищи и питательных веществ. — Головной офис: Лондон, 2007.
6.Рост и развитие недоношенных детей, вскармливаемых смесями с содержанием длинноцепочечных полиненасыщенных жирных кислот: проспективное, рандомизированное контролируемое исследование / O’Connor D. L. [et al.] // Pediatrics. — 2001. — Vol. 108. — P. 359—371.
7.Незаменимые n-3 жирные кислоты в питании беременных женщин и ранее созревание органов зрения у доношенных детей / Innis S. M. [и др.] // Американский журнал клинического питания. — 2008. — № 87. — С. 548—557.
8.Пищевые добавки с рыбьим жиром во время беременности регулируют аллергические реакции у младенцев и определяют клинический исход у детей с высоким риском атопических реакций: рандомизированное контролируемое исследование / Dunstan J. [et al.] // Journal of Allergy and Clinical Immunology. — 2003. — Vol. 112. — P. 1178—1184.
9.Пищевые добавки с рыбьим жиром при беременности и лактации могут снизить риск развития аллергии у детей / Furuhjelm C. [et al.] // Acta Paediatrica. — 2009. — Vol. 98. — P. 1461—1467.
10.Оценка когнитивной функции детей в возрасте 2(1/2) лет после того, как их матери во время беременности употребляли пищевые добавки с рыбьим жиром: рандомизированное контролируемое исследование / Dunstan J. A. с соавт. // Archives of Disease in Childho-od Fetal Neonatal Edition. — 2008. — Vol. 93. — P. 45—50.
11. Питание во время беременности с докозагексаеновой кислотой оказывает положительное воздействие на развитие зрения младенцев в возрасте 4 месяцев / Judge M. P. [et al.] // Lipids. — 2007. — Vol. 42. — P. 117—122.
12. Двойное слепое, плацебо контролируемое исследование действия пищевых добавок с омега-3 ЖК на детей в возрасте 8—10 лет / Kirby A. [et al.] // Research in Developmental Disabilities. — 2010. — Vol. 31. — P. 718—730.
13. W orld Association of Perinatal Medicine Dietary Guidelines Working Group.The roles of long-chain polyunsaturated fatty acids in pregnancy, lactation and infancy: review of current knowledge and consensus recommendations / Koletzko B., Lien E., Agostoni C. [et al.] // J. Perinat.
Med. — 2008. — Vol. 36 (1). — P. 5—14.
Жирно-кислотный спектр крови и пути коррекции его нарушений у детей раннего возраста с пищевой аллергией
О.Г. Шадрин, Г.А. Гайдучик
ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», г. Киев, Украина
Цель: исследование жирнокислотного спектра липидной фракции крови у детей раннего возраста с пищевой аллергией (ПА) и эффективности диетической коррекции его нарушений.
Пациенты и методы. Обследовано 45 детей в возрасте от 6-ти месяцев до 3-х лет. Всем детям проводилось исследование жирнокислотного спектра липидной фракции крови. Дети с ПА (25 чел) в составе комплексной терапии получали Смарт Омега® беби в течение месяца.
Результаты. По результатам анализа жирнокислотного спектра липидной фракции цельной крови у детей с ПА установлен дисбаланс жирных кислот за счет увеличения доли омега-6 ПНЖК, что свидетельствует о провоспалительной направленности обмена липидов. Включение в состав комплексной терапии ПА Смарт Омега® беби привело к положительным изменениям соотношения омега-3/омега-6 ПНЖК. У пациентов основной группы наблюдения произошло уменьшение расстройств со стороны желудочнокишечного тракта, улучшение состояния кожи.
Выводы. Учитывая выявленные нарушения соотношения омега-3/омега-6 ПНЖК как у детей с ПА, так и у практически здоровых обоснован приём омега3 ПНЖК.
Ключевые слова: пищевая аллергия, полиненасыщенные жирные кислоты, дети раннего возраста.
The ways of correction of fatty-acid profile of the blood in infants with food allergies
O.G. Shadrin, G.A. Gayduchik
SI «Institute of Pediatrics, Obstetrics and Gynecology NAMS of Ukraine», Kiev, Ukraine
Objective: Examination of the fatty-acid profile of the lipid fraction of blood in infants with food allergy (FA) and the effectiveness of dietary correction of violations.
Patients and methods. The study involved 45 children in the age from 6 months to 3 years. All children underwent examination of the fatty-acid profile of the lipid blood fractions. A total of 25 children with FA in the complex therapy had received a dietary supplement «Smart omega® baby lemon» within a month.
Results. According to the results of analysis of the fatty-acid profile of the lipid blood fraction in children with FA was found a fatty acids imbalance due to the increasing of the proportion of omega-6 PUFA, which is certifies about the proinflammatory direction of lipid metabolism. The inclusion to the complex therapy FA dietary supplement «Smart omega® baby lemon» has led to positive changes in the ratio of omega-3 / omega-6 PUFAs. In patients of the main group of observation was marked a reduction of disorders of the gastrointestinal tract and skin improvement.
Conclusions. For infants was recommended application of preparations containing omega-3 PUFAs taking into account the identified violations of the ratio of omega-3 / omega-6 PUFA as in children with FA so in practically healthy.
Key words: food allergy, polyunsaturated fatty acids, infants.




