Т.В. Марушко, О.Б. Герман, О.В. Олексенко
Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ, Україна
SOVREMENNAYA PEDIATRIYA.2017.5(85):94-109; doi 10.15574/SP.2017.85.94
У статті узагальнено дані літератури та власні спостереження щодо клініки, діагностики та лікувально-реабілітаційних заходів у дітей із гіпермобільним синдромом на тлі недиференційованої дисплазії сполучної тканини. Від особливостей сполучної тканини залежать процеси адаптації організму, стабільність його органів і систем, а розуміння особливостей метаболізму сполучної тканини та раннє виявлення його порушень може скласти основу профілактики багатьох дисфункцій і хронічних патологічних станів. Тому діти з гіпермобільним синдромом та ознаками недиференційованої дисплазії сполучної тканини повинні проходити комплексне обстеження для встановлення функціональних змін з боку органів та систем, що забезпечить своєчасне призначення профілактичних заходів, а за потреби — адекватного лікування.
Ключові слова: гіпермобільний синдром, діти, недиференційована дисплазія сполучної тканини.
Вступ
Загальновідомо, що стан довкілля і спосіб життя дитини мають вплив на формування її здоров’я. Розвиток дитячого організму може відбуватися у несприятливих умовах навколишнього середовища, супроводжуватися значним фізичним, психологічним та емоційним навантаженням, що може призводити у тому числі й до частих респіраторних захворювань. Цим пояснюється підвищення частоти соматичної патології (нервової, серцево-судинної системи, шлунково-кишкового тракту) та дисфункцій окремих органів у дитячого населення. Передусім це стосується дітей з особливостями конституції, зокрема з дисплазією сполучної тканини (ДСТ), що характеризується генетичними порушеннями в розвитку сполучної тканини (дефектами волокон колагену, еластину, глікопротеїдів, протеогліканів і фібробластів), в основі яких лежать успадковані мутації генів, що кодують синтез і просторову організацію колагену, структурних білків і білково-вуглеводних комплексів, а також мутації генів, що кодують різні ферменти і кофактори до них [1,5,11]. Від особливостей сполучної тканини залежать процеси адаптації організму, стабільність його органів і систем, а розуміння особливостей метаболізму сполучної тканини та раннє виявлення його порушень може скласти основу профілактики багатьох дисфункцій і хронічних патологічних станів.
Прояви ДСТ дуже різноманітні і не мають чітких клінічних ознак. Фенотипові ознаки ДСТ дуже різноманітні, вони вивчаються та доповнюються [5].
У клінічній практиці зазвичай лікар орієнтується на фенотипові ознаки недиференційованної дисплазії сполучної тканини (НДСТ), які зустрічаються у від 30% до 50% дітей (табл.1).
Окрім фенотипових ознак НДСТ існують особливості структури та функції внутрішніх органів. Дефекти у кожного хворого унікальні, при цьому всеосяжне поширення в організмі сполучної тканини визначає поліорганність уражень при ДСТ.
Одним із проявів ДСТ є гіпермобільний синдром (ГС), з яким досить часто стикаються лікарі-педіатри, сімейні лікарі, дитячі кардіоревматологи.
Мета роботи: узагальнення даних літератури та особистих спостережень щодо клініки, діагностики та лікувально-реабілітаційних заходів у дітей з ГС на тлі НДСТ.
Гіпермобільний синдром — системна особливість складу сполучної тканини, характеризується синдромом гіпермобільністі суглобів (СГМС), який поєднується зі скаргами з боку опорно-рухового апарату у вигляді артралгій, внутрішніми і зовнішніми фенотиповими ознаками ДСТ за відсутності ознак ревматичного захворювання [2,9,18]. В основі патогенезу ГС лежить спадковий дефект колагену, що супроводжується збільшенням розтягування і зменшенням механічної міцності структур сполучної тканини, які входять до складу зв’язок, ентезисів, сухожиль, сполучнотканинних структур серця, і призводить до підвивихів і мікротравматизації суглобового апарату, порушення роботи клапанного апарату та серцевого м’яза.
Клінічні прояви ГС різноманітні і включають як суглобові, так і позасуглобові ознаки [2].
Синдром гіпермобільності суглобів, який є першою ознакою ГС — це стан, при якому амплітуда рухів у суглобах дитини перевищує норму [2,9]. Поширеність цього стану у дітей залежить від віку [8,9,14]. У дітей перших тижнів життя ГС виявляти неможливо у зв’язку з гіпертонусом м’язів. У середньому ГС зустрічається у 71% дітей дошкільного віку та у 31,1% школярів, що становить 35–40% у дітей молодшого шкільного віку, відзначається у кожної четвертої дитини 13–15 років і кожної десятої 16–17 років. У маленьких дітей цей синдром зустрічається з рівною частотою у хлопчиків та дівчаток, а в пубертатному періоді — частіше у дівчаток. Поширеність цього стану в дорослій популяції становить 10–20% [2,18].
Для встановлення СГМС використовуються критерії P. Beighton (1998):
- пасивне згинання метакарпального суглоба V пальця на 90° в обидві сторони (1–2 бали);
- пасивне згинання I пальця в бік передпліччя при згинанні в променево-зап’ястковому суглобі (1–2 бали);
- перерозгинання обох ліктьових суглобів >10 градусів (1–2 бали);
- перерозгинання обох колінних суглобів >10 градусів (1–2 бали);
- при нахилі вперед при фіксованих колінних суглобах долоні торкаються підлоги (1 бал).
Гіпермобільність оцінюють у балах:
- 1 бал означає патологічне перерозгинання суглоба на одній стороні;
- максимальна величина показника, враховуючи двосторонню локалізацію, — 9 балів (8 — за 4 перші пункти і 1 — за 5-й пункт).
- показник гіпермобільності має декілька ступенів: легкий — 3–4 бали, середній — від 4 до 8 балів, виразна гіпермобільність — 9 балів.
Гіпермобільність суглобів є фактором ризику виникнення м’язово-суглобового больового синдрому, підвивихів, раннього остеоартрозу.
Артралгії найчастіше зустрічаються з локалізацією в колінних і гомілковостопних суглобах, частіше асоційовані з фізичним навантаженням. Причиною больового синдрому на тлі ГС є зміна чутливості пропріорецепторів до навантаження суглобів [6]. При тривалих артралгіях можлива поява ознак рецидивного синовіту опорних суглобів у зв’язку з порушенням фізіологічної вісі суглоба та неправильним навантаженням суглобових структур [10].
Характерною особливістю синовіту є безпосередній зв’язок із травмою та/або надмірним навантаженням, а також відсутність системної запальної реакції. У дітей можуть спостерігатися ознаки дорсалгій із локалізацією в поперековому і грудному відділах хребта, які виникають у другій половині дня, після тривалих статичних навантажень, при неправильній позі за шкільною партою [3]. Недостатність сполучнотканинного фіксуючого апарату хребта під впливом несприятливих факторів тягне за собою компенсаторний розвиток деформацій хребта (сколіоз) з подальшим посиленням больового синдрому [14]. Також у відповідь на незвичне навантаження або мінімальну травму у пацієнтів виникають симптоми періартикулярного ураження (тендиніти, епікондиліти, ентезопатії, бурсити). Слід зазначити, що артралгії при СГМС не піддаються знеболювальній дії нестероїдних протизапальних препаратів, що вказує на їх незапальний характер. При огляді потенційно ураженого суглоба зазвичай будь-яких об’єктивних ознак патології не виявляється. Цей факт може бути використаний в якості диференційно-діагностичної ознаки, що відрізняє біль при СГМС від запальних артропатій [10].
Брайтонські критерії (1998) ГС Graham у модифікації А.Г. Беленького (2004), які найбільш доцільно використовувати для встановлення діагнозу у дітей, наведені у таблиці 2.
Гіпермобільний синдром діагностується за наявності 2 великих критеріїв або 1 великого і 2 малих критеріїв, або 4 малих. Гіпермобільний синдром діагностується при наявності 2 малих критеріїв, якщо має місце захворювання у родича першого ступеня споріднення.
Гіпермобільний синдром виключається за наявності ознак синдрому Марфана або синдрому Елерса—Данло, або будь-якого ревматичного захворювання. Критерії великий 1 та малий 1 виключають один одного, так само як великий 2 і малий 2.
Частою скаргою у дітей з СГМС, особливо підліткового віку, є хрускіт або клацання в суглобах (звукові феномени гіпермобільності).
Ці явища добре вислуховуються, безболісні і носять множинний характер, що говорить про їх доброякісність та відрізняє від патологічного хрускоту, який спостерігається при запальних артропатіях [5]. Поява клацань при СГМС зазвичай пов’язана зі зміною режиму фізичного навантаження, передбачає участь м’язового компоненту та гіпереластичного зв’язкового апарату в ґенезі даного феномена (ослаблення м’язів призводить до порушення стабілізації суглоба, гіпереластичність зв’язок — до підвивихів).
Одним із проявів ГС є клапанний синдром: ізольовані і комбіновані пролапси клапанів серця (найчастіше — пролапс мітрального клапана, 70%). Пролапс мітрального клапана (ПМК) визначається за даними еходопплеркардіографії як провисання однієї або обох стулок мітрального клапана в порожнину лівого передсердя на 2 мм і більше над рівнем мітрального кільця по горизонтальній осі в парастернальній позиції з можливою міксоматозною дегенерацією стулок або без неї, з мітральної регургітацією або без неї (ACC/AHA, RO Bonow, 2006). Пролапс мітрального клапана при ДСТ формується як генетично детермінований дефект синтезу колагенових і еластичних структур, відкладення в стромі клапана глікозоаміногліканів [4].
У дітей клінічні прояви ПМК спостерігаються від мінімальних до значних і визначаються ступенем сполучнотканинної дисплазії серця, вегетативними і психоневрологічними відхиленнями. У більшості дітей визначаються різноманітні скарги на біль у грудній клітці, періодичне серцебиття, задишку, слабкість, можливе запаморочення. Біль у серці має переважно колючий характер, триває протягом 5–20 хвилин, виникає у зв’язку з емоційною напругою і супроводжується, як правило, вегетативними порушеннями: нестійким настроєм, похолодінням кінцівок, серцебиттям. При ПМК у дітей досить часто зустрічається порушення серцевого ритму, виявлення якого потребує проведення добового холтерівського ЕКГ-моніторингу. Серед аритмій у дітей з ПМК найчастіше виявляються синусова тахікардія, надшлуночкові і шлуночкові екстрасистолії, рідше — брадикардія [15].
На базі кардіоревматологічного відділення Київської міської дитячої клінічної лікарні №1 був проведений аналіз клінічних ознак ГС на тлі НДСТ у 54 дітей. Діти скаржилися на періодичний біль у ділянці серця, відчуття серцебиття, швидку втомлюваність, слабкість, періодичний головний біль, запаморочення, артралгії (табл. 3). Частота клінічних ознак при ГС у дітей відображена в таблиці 4.
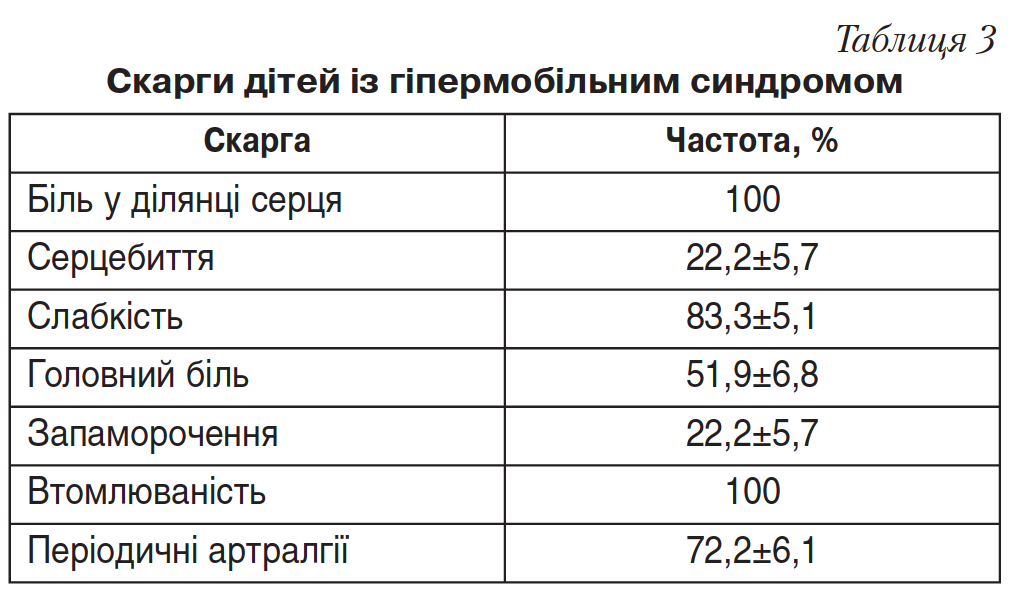
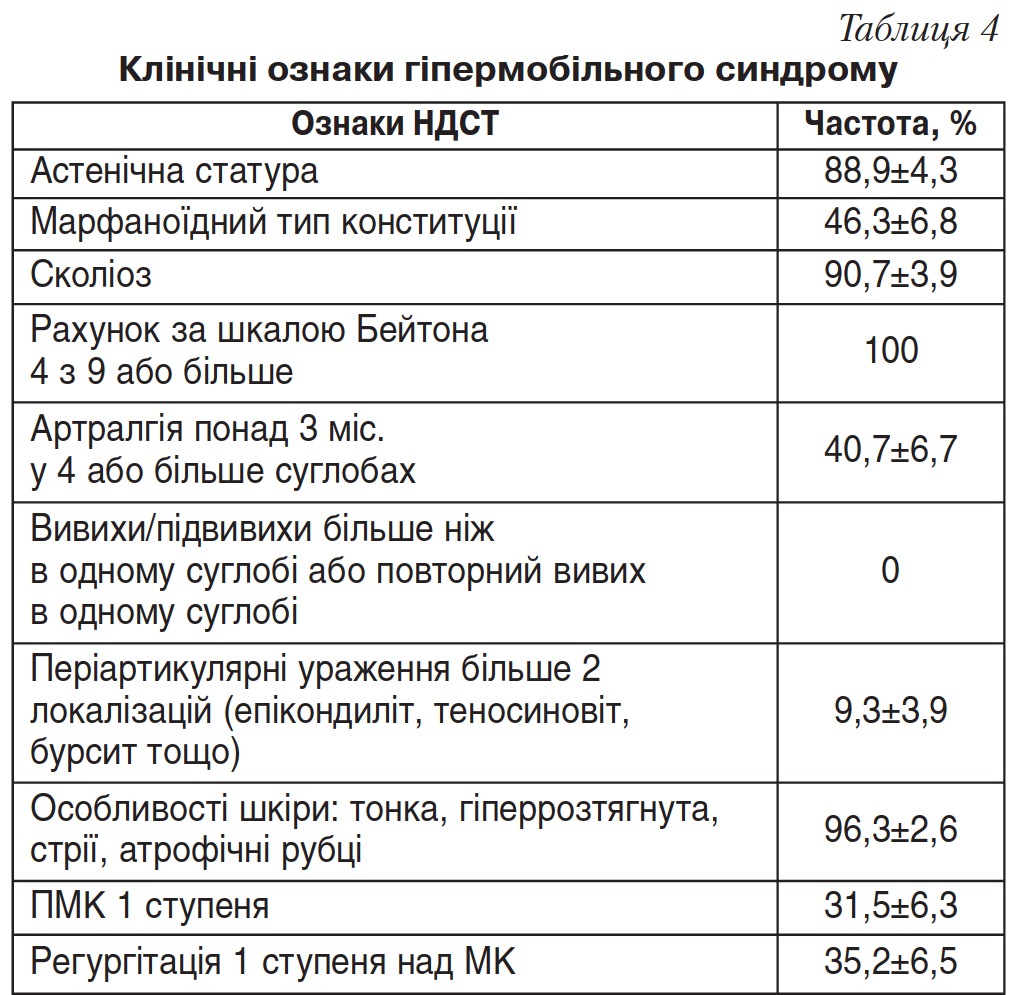
Усі діти були обстежені клінічно, лабораторно, інструментально. Лабораторне обстеження включало загальний аналіз крові, загальний аналіз сечі, біохімічне дослідження сироватки крові та аналіз ревмопроб. Для характеристики функціонального стану серцево-судинної системи проводили електрокардіографію, добовий Холтер-моніторинг ЕКГ. Показники гемодинаміки аналізували за даними ехокардіографії (ЕхоКГ).
Із об’єктивних показників контролювали динаміку частоти серцевих скорочень (ЧСС), кількість екстрасистол за добу, зміни сегменту SТ та QТ, які відображають процес реполяризації у міокарді, скоротливу функцію міокарда за даними ЕхоКГ. Дітям з артралгіями проводили ультразвукове обстеження суглобів.
Дослідження виконані відповідно до принципів Гельсінської Декларації. Протокол дослідження ухвалений Локальним етичним комітетом (ЛЕК) установи. На проведення досліджень було отримано поінформовану згоду батьків дітей (або їхніх опікунів).
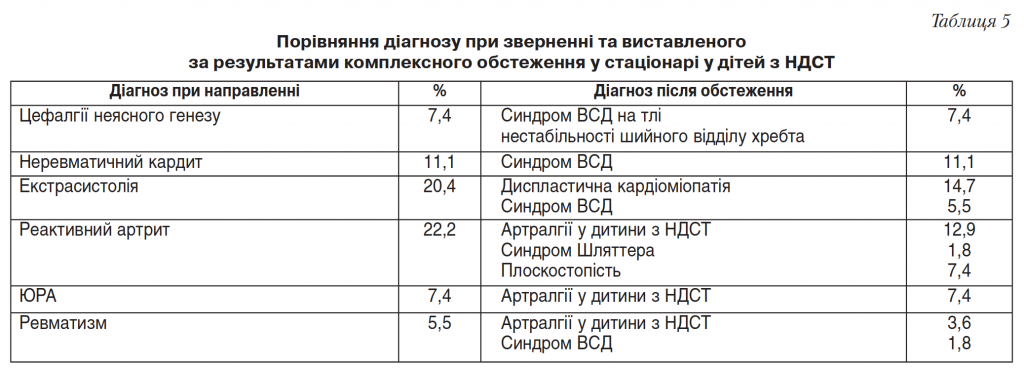
Ми проаналізували збіг діагнозів при направленні дітей у стаціонар (на консультацію) та діагнозів, які були виставлені після клінічного обстеження на фоні ГС (табл. 5). Таким чином, ГС є одним з проявів ДСТ, а його складові можуть бути «масками» органічної патології у дітей. В організмі дитини він створює умови для розвитку деформування, дезорганізації тканинних структур, процесів метаболізму органів і систем, опорно-рухового апарату. У процесі спостереження прояви ГС зазвичай прогресують і можуть лежати в основі формування соматичної патології, що вимагає своєчасної клінічної оцінки та лікувально-профілактичних заходів. Попри те, що ГС є дуже поширеним проявом ДСТ, рівень доказовості його корекції є недостатнім. Аналіз рекомендацій щодо корекції способу життя, фізичних навантажень доводить той факт, що кожній дитині з ГС повинна бути розроблена індивідуальна програма з харчування, денного розкладу, режиму навчання, фізичної активності [10,11].
З огляду на патогенетичну основу слабкості сполучної тканини і багатофакторний характер проявів при ГС, одним з важливих напрямків впливу на його прояви є корекція порушеного метаболізму колагену, функції фібробластів та інших компонентів сполучної тканини. Показані курси основних груп препаратів, які прямо або опосередковано впливають на метаболізм сполучної тканини. Їх поділяють на декілька груп [8]:
- препарати, що сприяють колагеноутворенню і підтримці окисно-відновних процесів (аскорбінова кислота, вітаміни групи В (В1, В2, фолієва кислота, В6), мікроелементи у вигляді Cu2+, Zn2+, Mg2+, Mn2+;
- препарати, які сприяють корекції порушень синтезу і катаболізму глюкозаміногліканів — хондропротектори;
- препарати, які стабілізують фосфорно-кальцієвий мінеральний обмін (Са2+ та вітамін D);
- коректори біоенергетичного стану організму — препарати аденозинтрифосфорної кислоти, препарати поліненасичених жирних кислот.
У наш час широко обговорюється роль дисмікроелементозів у порушенні функції сполучної тканини: недостатній вміст мікроелементів, порушення їх обміну викликає порушення процесів обміну сполучної тканини, при дефіциті магнію знижується здатність фібробластів продукувати колаген. Ремоделізація кісткової тканини страждає при недостатності кальцію та вітаміну D3. Однак кальцій є антагоністом магнію — проколагенового препарату, тому при надмірній дозі цього препарату порушується їх співвідношення, що забезпечує неадекватне утворення кісткової тканини (співвідношення кальцію і магнію у дітей має бути 2:1). Незбалансоване харчування може стати причиною негативного балансу кальцію і магнію в організмі і призвести до ще виразнішого розладу метаболізму в кістках та тканинах [6].
Серед коректорів біоенергетичного стану організму слід звернути увагу на препарати поліненасичених жирних кислот (ПНЖК), які мають багатофакторний вплив на дисфункцію органів та систем при ГС [18]. Дітям з надмірно високим зростом та ГС вже з раннього віку рекомендуються продукти харчування (соєва, бавовняна, оливкова олія, насіння соняшника), а також препарати з підвищеним вмістом ПНЖК класу омега-3, що мають гальмівний ефект на секрецію соматотропного гормону, сприяючи рівномірному зростанню дитини.
Призначення вітамінів (С, А, Е), ПНЖК, які входять до складу омега-3, показане для нормалізації процесів перекисного окислення.
Протизапальна дія омега-3 ПНЖК забезпечує позитивний ефект при артралгіях у дітей з НДСТ, відчуття болю при яких може виникати в результаті мікротравм зв’язок при нестабільності періартикулярних тканин дитини [12].
Оскільки омега-3 ПНЖК впливають на гуморальні та клітинні ланки імунітету, показане їх включення в комплексне профілактичне лікування дітей, що часто хворіють, на тлі ГС. Протидія омега-3 ПНЖК прозапальним ефектам метаболітів арахідонової кислоти (простациклін, лейкотрієни та інші) пояснює їх лікувальну та профілактичну дію.
Омега-3 ПНЖК впливають на електричну нестабільність міокарда. Атиаритмічна дія омега-3 ПНЖК полягає в молекулярно-специфічному пригніченні трансмембранних каналів, у результаті чого подовжується неактивна фаза та порогові рівні деполяризації у кардіоміоцитах, що сприяє зменшенню явищ екстрасистолії.
Цікаві експериментальні дані про те, що до порушення ритму серця можуть призводити зміни складу жирних кислот фосфоліпідів внутрішніх органів: збільшення частки насичених і зниження ПНЖК, причому серце є органом, в якому ці зміни виражені максимально. Зростаючий організм дитини найбільш чутливий до дефіциту ПНЖК, оскільки більше потребує пластичного матеріалу для синтезу фосфоліпідів, які є важливим джерелом енергії для будь-якого організму.
Ряд дослідників вважають, що одним із факторів ушкодження органів та тканин у стресорних ситуаціях, до яких можна віднести ГС, поряд зі значним енергетичним дефіцитом, є дисбаланс синтезу та розпаду білків, а фактори, що призводять до цього, — гіперактивація симпатико-адреналової системи [19]. Адренореактивні системи здатні динамічно змінюватися під впливом таких факторів, як гіпоксія, коливання температури, порушення метаболічної активності, гормонального статусу, а вплив кожного з цих факторів опосередкований порушенням фосфоліпідного складу мембран. Омега-3 ПНЖК є основним компонентом фосфоліпідів клітинних мембран, що визначає рідкокристалічні властивості і проникність останніх.
Виходячи з вищезазначеного, нами дітям з ГС, разом з індивідуальними рекомендаціями щодо харчування, способу життя, фізичних навантажень, був призначений препарат омега-3 ПНЖК. Препарат призначався дітям віком до 7 років по 1 капсулі на добу під час їжі; дітям віком 7–14 років — по 2 капсули на добу під час їжі протягом одного місяця на квартал.
Позитивна динаміка була отримана в 88,9±4,3%, що свідчить про необхідність подальшого вивчення впливу омега-3 ПНЖК на клінічні прояви ГС.
Висновки
Таким чином, діти з ГС та ознаками НДСТ повинні проходити комплексне обстеження для встановлення функціональних змін з боку органів та систем, що забезпечить своєчасне призначення профілактичних заходів, а за потреби — адекватного лікування. Потрібне подальше вивчення впливу омега-3 ПНЖК як профілактичного та лікувального засобу функціональних розладів органів та систем, які спостерігаються у дітей із ГС на тлі НДСТ.
Автори заявляють про відсутність конфлікту інтересів.
ЛІТЕРАТУРА
1. Абакумова Л.Н. Клинические формы дисплазии соединительной ткани у детей / Л.Н. Абакумова. — Санкт-Петербург, 2006. — 36 с.
2. Беленький А.Г. Гипермобильность суставов и гипермобильный синдром: распространенность и клинико-инструментальная характеристика: дис. … д-ра мед. наук / А.Г. Беленький. — Москва, 2004. — 249 с.
3. Гипермобильность суставов и гипермобильный синдром – клинические аспекты / Шостак Н.А., Правдюк Н.Г., Тимофеев В.Т., Шеметов Д.А. // Поликлиника. — 2017. — №1. — С.49—52.
4. Земцовский Э.В. Соединительнотканные дисплазии сердца / Э.В. Земцовский. — Политекс-Норд-Вест, 2000. — 115 с.
5. Кадурина Т.И. Дисплазия соединительной ткани: руководство для врачей / Т.И. Кадурина, В.Н. Горбунова. — Санкт-Петербург: Элби-СПб., 2009. — 704 с.
6. Кравченко А.И. Недифференцированная дисплазия соединительной ткани опорно-двигательной системы (диагностика, лечение) / А.И. Кравченко // Травма. — 2014. — №1, Т.15. — С.118—124.
7. Кулешов А.В. Состояние вегетативной нервной системы у детей с недифференцированной дисплазией соединительной ткани / Кулешов А.В. // Педиатрия. — 2017. — №3. — С.101—106.
8. Поворознюк В.В. К вопросу о синдроме гипермобильности суставов / В.В. Поворознюк, Е.И. Подлианова // Боль, суставы, позвоночник. — 2012. — №1 (05). — С.33—35.
9. Распространенность гипермобильности суставов в детской популяции Твери / Иванова И.И., Гнусаев С.Ф. [и др.] // Вестник северо-западного гос. мед. ун-та. — 2013. — Т.5, №4. — С.94—10
10. Сатыбалдыев А.М. Синдром гипермобильности суставов в ревматологии / А.М. Сатыбалдыев // Современная ревматол. — 2017. — №11(2). — С.68—74.
11. Тябут Т.Д. Недифференцированная дисплазия соединительной ткани [Электронный ресурс] / Т.Д. Тябут, О.М. Каратыш // Совре-менная ревматол. — 2009. — №2. — URL: http://cyberleninka.ru/ar-ticle/n/nedifferentsirovannaya-displaziya-soedinitelnoy-tkani.
12. Шевелёк А.Н. Влияние омега-3 полиненасыщенных жирных кислот на биоэлектрическую активность сердца у пациентов с пароксизмальной фибрилляцией предсердий / А.Н. Шевелёк // Український кардіолог. журн. — 2014. — №2. — С.93—99.
13. Ярема Н.М. Применение омега-3 полиненасыщенных жирных кислот для оптимизации лечения воспалительных заболеваний суставов у детей / Ярема Н.М. // Вопросы питания. — 2017. — №2. — С.84—90.
14. Epidemiology of generalized joint laxity (hypermobility) in fourteen-year-old children from the UK: a population-based evaluation / Clinch J., Deere K., Sayers A. [et al.] // Arthritis Rheum. — 2011. — Vol. 63(9). — P. 2819—27.
15. Fu Q. Exercise in the postural orthostatic tachycardia syndrome / Q. Fu, B.D. Levine // Autonomic Neuroscience: Basic and Clinical. — 2015. — Vol.188. — P.86—89.
16. Graham R. The British Society for Rheumatology Special Interest Group on Heritable Disoders of Connective Tissue. Criteria for the Benign Joint Hypermobility Syndrome. The Revised (Brighton 1998) Criteria for the Diagnosis of the BJHS / R. Graham, H. Bird, A. Child // J. Rheumatol. — 2000. — Vol.27. — 1777—9.
17. Joint hypermobility in children with idiopathic scoliosis: SOSORT award 2011 winner / Czaprowski D., Kotwicki T. [et al.] // Scoliosis. — 2011. — Vol.7. — P.6—22.
18. Neki N.S. Benign joint hypermobility syndrome / N.S. Neki, A. Chhabra // J. Mahatma Gandhi Inst Med Sci. — 2016. — Vol.21. — Р.12—18.
19. Physiotherapy management of joint hypermobility syndrome — a focus group study of patient and health professional perspectives / Palmer S. [et al.] // Physiotherapy. — 2016. — Vol.102. — P.93—102.
Відомості про авторів:
Марушка Тетяна Вікторівна – д.мед.н., проф., завідувач кафедри педіатрії-2 Національної медичної академії післядипломної освіти імені П.Л. Шупика. Адреса: м. Київ, Дорогожицька, 9
Герман Олена Борисівна – к.мед.н., лікар-педіатр, лікар – дитячий кардіоревматолог, лікар ультразвукової діагностики, асистент кафедри педіатрії-2, Національної медичної академії післядипломної освіти імені П.Л. Шупика. Адреса: м. Київ, Дорогожицька, 9
Олексенко О.В. – лікар-кардіоревматолог, завідувач відділення кардіоревматології КДДКБ №1.
Стаття надійшла до редакції





